近年来,水凝胶材料与生物组织的强韧粘接技术受到广泛关注。然而,对于新开发的水凝胶粘接剂和粘接技术,能否用于实际临床手术环境非常关键。如何将水凝胶应用于外科手术,进而研究水凝胶在生物体内的反应,改进水凝胶的材料设计,成为当下研究的热点。
近日,西安交通大学第一附属医院吕毅教授、航天航空学院唐敬达副教授以及哈佛大学锁志刚教授等人,提出磁辅助-水凝胶粘接方法,成功应用于大动物的肝移植手术中, 术后动物恢复良好,血管完全愈合。研究成果以Adhesive anastomosis for organ transplantation为题发表在生物医学领域顶级期刊《Bioactive Materials》(影响因子14.593)。

血管缝合法与“磁辅助-水凝胶粘接”血管吻合法
血管吻合技术从Alexis Carrel发明“三点式”血管缝合法后(1912年诺贝尔生理学或医学奖),至今已超过100年的历史。血管缝合法具有许多优势,但是操作复杂、缝合时间长。肝移植过程中,需要吻合三根大血管,吻合过程中下肢血液无法经肝脏回流到心脏,称为“无肝期”,无肝期越长,患者愈后越差。对于“争分夺秒”的肝脏移植手术来讲,传统“一针一线”式的手工缝合法显然无法满足医生和患者的需求,亟需一种新型的血管吻合技术。
本工作使用强韧可降解水凝胶粘接技术,用于器官移植过程中的血管吻合。血管外翻后,该粘接技术作用于血管内皮以保证血管重建。初始阶段借助于两端血管磁环相互作用,使血流在短时间恢复流动;水凝胶粘接逐渐与血管内皮形成强共价键。撤去磁环后,水凝胶粘接维持正常血压。随着血管内皮的再生,水凝胶逐渐降解并最终完成血管重建(图1)。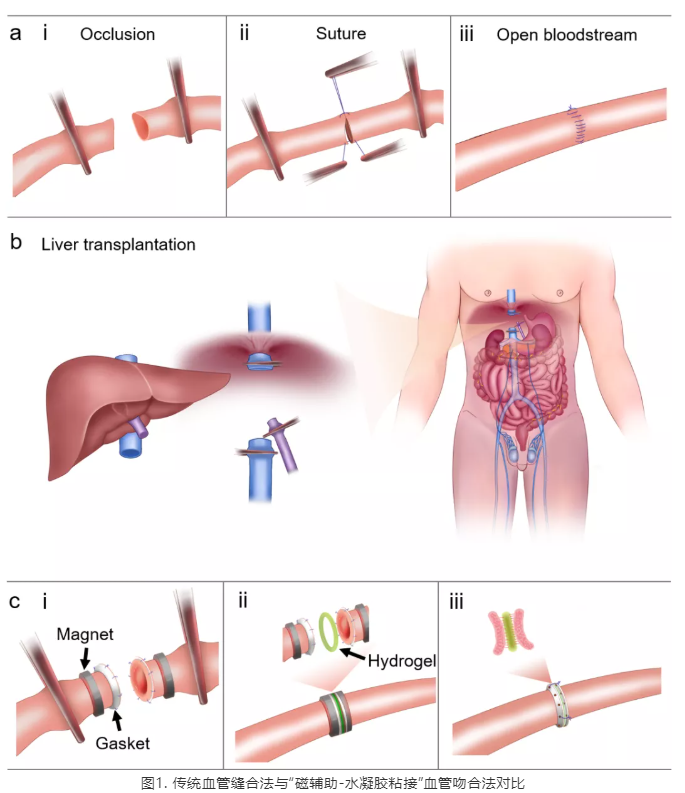
本文采用的水凝胶由双层网络组成(图2):由钙离子交联的海藻酸钠网络和由二硫键交联的聚丙烯酰胺网络。胶水为壳聚糖、EDC/NHS 的水溶液, 使用时胶水施加在水凝胶与组织之间,促进共价键的形成。该水凝胶强韧粘接原理是:在 EDC/NHS 作用下,壳聚糖上的胺与组织和藻酸盐上的羧基形成肽键,壳聚糖充当组织和水凝胶之间的桥接聚合物。在剥离过程中,钙离子交联的海藻酸钠网络具有耗散作用,强粘接层与水凝胶耗散作用产生高粘接能。该水凝胶的降解原理是:体液中的钠离子与钙离子交换可以降解海藻酸钠的交联网络;体液中的还原作用如半胱氨酸与二硫键反应可以降解聚丙烯酰胺的交联网络。本文重点介绍这种水凝胶在血管吻合术中的应用。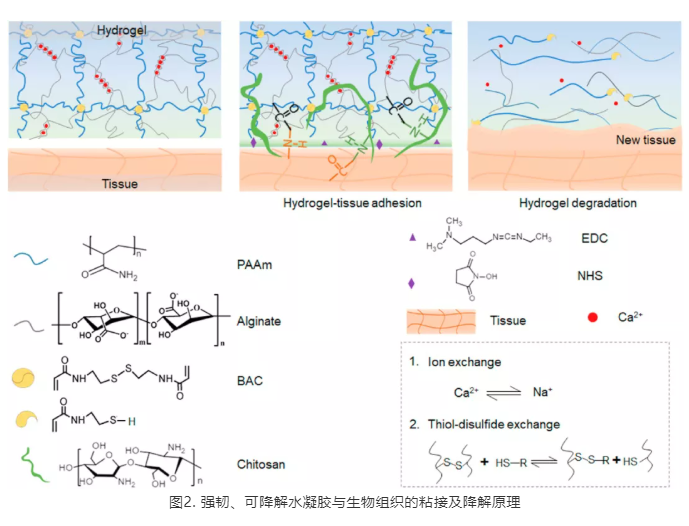
作者首先开展了体外实验,测量了水凝胶与血管组织的粘接强度,耐水流测试、爆破压测试,吻合时间测试。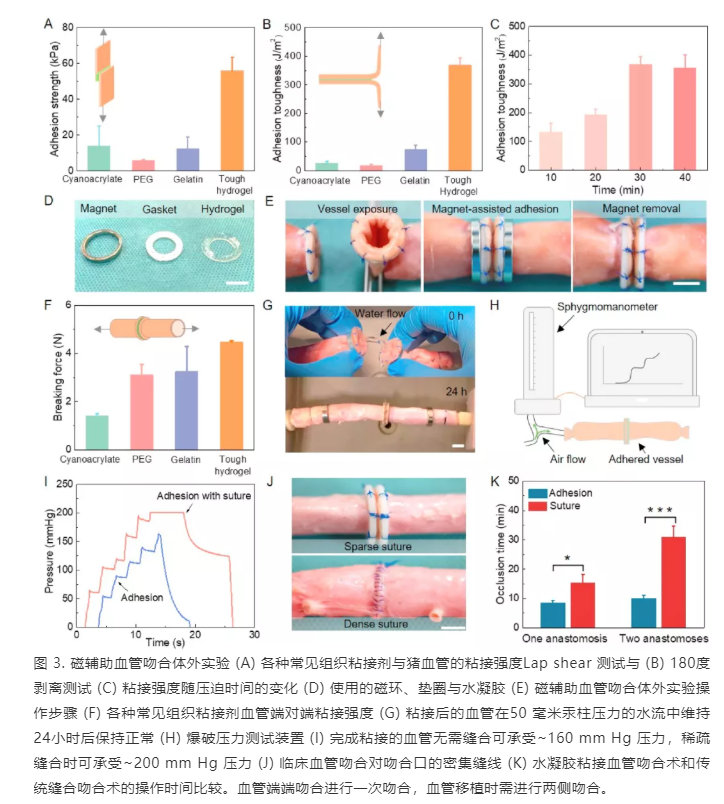
本研究发现水凝胶对人脐静脉内皮细胞没有毒性,不会引起人外周血单核细胞的炎症反应发生,在动物体内的组织相容性良好,放置一个月后水凝胶可以完全降解,动物组织可以完全愈合。
本研究在大动物肝脏移植模型上成功实现了磁辅助-水凝胶粘接血管吻合,术后实验动物恢复良好,肝功能在第8天完全恢复正常。术后38天,对动物尸体进行解剖,结果表明磁辅助-水凝胶吻合的血管完全愈合,无狭窄或血栓等并发症发生。
论文第一作者为西安交通大学2018级外科学博士刘康(现就职于西安交通大学第一附属医院),共同第一作者为西安交通大学航天航空学院硕士生杨航(现为哈佛大学在读博士)以及西安交通大学2019级外科学硕士生黄高铂。通讯作者为哈佛大学锁志刚教授、西安交通大学唐敬达副教授和西安交通大学第一附属医院吕毅教授。Bioactive Materials为生物医学领域顶级期刊,最新影响因子为14.593。
研究受“陕西省2020年重点研发计划”项目、国家自然科学基金面上项目资助,苏州茵络医疗器械有限公司及苏州凝智新材料发展有限公司提供技术支持。
论文链接:
https://www.sciencedirect.com/science/article/pii/S2452199X21005247

 塑库专家服务
塑库专家服务
 新品选材
新品选材
 3000+ 合作案例
3000+ 合作案例
 缺陷解决
缺陷解决
 专业团队1V1跟进
专业团队1V1跟进
 热门文章
热门文章